Metaal
Metaal wordt al eeuwenlang gebruikt en is één van de basismaterialen in ons heelal.
Het is een groep elementen die veelvuldig wordt toegepast in allerlei vormen, samenstellingen en producten. Bekende metalen zijn goud, aluminium en ijzer en staal. Niet alle metalen zijn in zuivere vorm verkrijgbaar, er is dan sprake van een legering. Binnen de werktuigbouwkunde spreken we ook bij legeringen nog altijd over metalen. Eén van de bekendste legeringen is staal, een combinatie van o.a. ijzer en koolstof.
De oorsprong van metalen
Het heelal bestaat uit een vrijwel oneindige hoeveelheid materie. Deze materie is opgebouwd uit elementen, een zuivere stof die niet langs chemische weg tot eenvoudige stof kan worden afgebroken. De elementen worden opgedeeld in twee groepen; organische- en anorganische stoffen. Metaal is een anorganische stof, die in de natuur zelden in zuivere vorm wordt gevonden. Metalen worden gedolven in de vorm van ertsen, die vervolgens worden omgezet in de zuivere metaalvorm. Vrijwel de enige metalen die in zuivere vorm gevonden worden, zijn edelmetalen vanwege hun zeer lage chemische reactiviteit.
In de scheikunde wordt het begrip metaalsoorten anders uitgelegd dan binnen de werktuigbouwkunde en metaalkunde.
Uitleg over het begrip metaal
Alle metalen zijn scheikundige elementen, deze staan vermeld in het periodiek systeem der elementen. Van de 90 stabiele elementen behoren er 65 tot de metalen.
De metalen worden opgedeeld in een aantal groepen:
Deze metalen hebben een hoge reactiviteit en verbinden zich makkelijk aan andere elementen.
In de natuur komt geen van deze elementen in zuivere vorm voor.
De elementen in de groep alkalimetalen zijn:
- Lithium (Li)
- Natrium (Na)
- Kalium (K)
- Rubidium (Rb)
- Cesium (Cs)
- Francium (Fr)
Een van de meest voorkomende alkalimetalen is natrium, wat onder andere in zout voorkomt (zout = natriumchloride). Alkalimetalen zijn zeer reactief met zuurstof en met water. Deze komen dan ook niet in zuivere vorm voor op aarde.
Aardalkalimetalen hebben een net als de alkalimetalen een hoge reactiviteit, maar zijn stabieler dan Alkalimetalen.
De elementen in de groep aardalkalimetalen zijn:
- Beryllium (Be)
- Magnesium (Mg)
- Calcium (Ca)
- Strontium (Sr)
- Barium (Ba)
- Radium (Ra)
Deze groep van metalen komen we regelmatig voor in legeringen die ook binnen Tosec veel gebruikt worden. Denk aan de aluminiumlegering AlMg3.
Beryllium wordt gebruikt in hoogwaardige luidsprekers. Bij de bouw van de hoge tonen luidsprekers (tweeters) wordt berylliumoxide gebruikt voor het produceren van zeer lichte conussen.
Strontium kan gebruikt worden voor het produceren van zeer sterke permanent-magneten.
In deze groep zitten alle elementen die gebruikt worden in de metaalbewerking zoals Titanium, Chroom, IJzer, Zink, Mangaan, Wolfraam, maar ook Zilver, Platina en Goud.
De elementen in de groep overgangsmetalen zijn:
- Scandium (Sc)
- Titanium (Ti)
- Vanadium (V)
- Chroom (Cr)
- Mangaan (Mn)
- IJzer (Fe)
- Kobalt (Co)
- Nikkel (Ni)
- Koper (Cu)
- Zink (Zn)
- Yttrium (Y)
- Zirkonium (Zr)
- Niobium (Nb)
- Molybdeen (Mo)
- Technetium (Tc)
- Cadmium (Cd)
- Hafnium (Hf)
- Tantaal (Ta)
- Wolfraam (W)
- Renium (Re)
- Kwik (Hg)
De volgende elementen vallen onder de edelmetalen en reageren bij kamertemperatuur niet of nauwelijks met zuurstof (oxideren):
- Ruthenium (Ru)
- Rodium (Rh)
- Palladium (Pd)
- Zilver (Ag)
- Osmium (Os)
- Iridium (Ir)
- Platina (Pt)
- Goud (Au)
De toepassing van deze elementen in metaallegeringen is, niet in het minst omdat ze radioactief zijn, minimaal tot nihil:
- Rutherfordium (Rf)
- Dubnium (Db)
- Seaborgium (Sg)
- Bohrium (Bh)
- Hassium (Hs)
- Meitnerium (Mt)
- Darmstadtium (Ds)
- Röntgenium (Rg)
- Copernicium (Cn)
Zeldzame aardmetalen of zeldzame aarden zijn 15 elementen uit de serie lanthanoïden en Scandium (Sc) en Yttrium (Y).
De 15 elementen die onder de lanthanoïden (Ln) vallen zijn:
- Cerium (Cr)
- Praseodymium (Pr)
- Neodymium (Nd)
- Promethium (Pm)
- Samarium (Sm)
- Europium (Eu)
- Gadolinium (Gd)
- Terbium (Tb)
- Dysprosium (Dy)
- Holmium (Ho)
- Erbium (Er)
- Thulium (Tm)
- Ytterbium (Yb)
- Lutetium (Lu)
Een bekend element uit deze reeks is Neodymium wat gebruikt wordt in zeer sterke permanentmagneten en in de magneten van high-end luidsprekers en de hogere kwaliteit hoofdtelefoons.
In tegenstelling tot wat de naam van de groep doet vermoeden zijn lang niet alle elementen zeldzaam. Meerdere elementen komen zelfs vaker voor op aarde dan veel meer gebruikte elementen. Zelfs het meest zeldzame element Lutetium (Lu) komt nog altijd vaker voor dan goud.
Luthetium wordt o.a. gebruikt in nucleaire geneeskunde bij de behandeling van kanker.
Cerium is een element wat in de vorm van ceriumoxide gebruikt wordt in de katalysator van benzineauto's om uitlaatgassen te zuiveren.
De groep Actinoïden bevat net als de groep Lanthanoïden 15 elementen. In het geval van de actinoïden zijn alle elementen radioactief.
Deze groep elementen bestaat uit:
- Actinium (Ac)
- Thorium (Th)
- Proactinium (Pa)
- Uranium (U)
- Neptunium (Np)
- Plutonium (Pu)
- Americium (Am)
- Curium (Cm)
- Berkelium (Bk)
- Californium (Cf)
- Einsteinium (Es)
- Fermium (Fm)
- Mendelevium (Md)
- Nobelium (No)
- Lawrencium (Lr)
Een aantal elementen zijn bekend van de koude oorlog waarin wereldwijd werd gedreigd met nucleaire wapens welke gebouwd konden worden met behulp van uranium en plutonium.
De laatste decennia wordt onderzocht of Thorium kan dienen als brandstof in een kernreactor om energie mee op te wekken.
In deze groep zitten nog enkele metalen die niet in de voorgaande groepen vallen om meerdere scheikundige redenen. De bekendste zijn Aluminium, tin en lood.
De elementen in de hoofdgroepmetalen zijn:
- Aluminium (Al)
- Gallium (Ga)
- Indium (In)
- Tin (Sn)
- Thallium (Tl)
- Lood (Pb)
- Bismut (Bi)
Van de volgende elementen valt te betwisten of ze onder de hoofdgroepmetalen vallen. De toepassing van deze elementen is op dit moment niet bewezen:
- Polonium (Po)
- Nohonium (Nh)
- Flerovium (Fl)
- Moscovium (Mc)
- Livermorium (Lv)
De groep metalloïden vormt een aparte groep met elementen die lijken op metalen maar niet aan alle kenmerken voldoen. Zo zijn enkele metalloïden halfgeleiders, wat inhoudt dat deze elementen slechts onder voorwaarden elektrisch geleidend zijn. Ze raken bijvoorbeeld pas geleidend bij hogere temperaturen.
De elementen in de groep metalloïden beperkt zich tot:
- Boor of Borium (B)
- Silicium (Si)
- Germanium (Ge)
- Arseen of Arsenicum (As)
- Antimoon of Antimonium (Sb)
- Telluur of Tellurium (Te)
4 Gemeenschappelijke kenmerken
Metalen hebben 4 kenmerkende eigenschappen welke zowel in vaste als in vloeibare vorm gelden:
- Elektrisch geleidend.
De elektronen, met name die in de buitenste schillen, zijn niet sterk verbonden aan de kern en kunnen daardoor gemakkelijk uitwisselen. - Hoge warmtegeleiding.
Metalen kunnen warmte snel transporteren. Metalen voelen bij kamertemperatuur dan ook koud aan omdat de warmte van je hand snel wordt afgevoerd. - Goede vervormbaarheid (ductiliteit).
Metalen kunnen goed vervormd worden. Een eigenschap waar wij binnen Tosec natuurlijk gebruik van maken tijdens het buigen. - Metalen reflecteren licht goed.
Metalen reflecteren licht goed. Dit geeft metalen hun kenmerkende glans. Met name metalen als RVS en edelmetalen worden hoogglans gepolijst voor hun toepassingen als sieraden of onderdelen op luxe schepen, jachten.
Metaaltypen
Metaalsoorten komen in twee typen voor; zowel in zuivere vorm als een combinatie van verschillende elementen.
Metaalsoorten met een zuivere vorm zijn; beryllium, titaan, koper, goud, zilver, platina, lood en kwik.
Het grootste deel van de metalen is echter alleen te realiseren wanneer een combinatie van verschillende elementen plaatsvindt. Er zijn drie soorten combinaties:
- Legeringen
Een combinatie van metalen en/of andere elementen. - Verbindingen
Een stof waarbij de elementen moleculen vormen met een vaste chemische samenstelling. - Mengsels
Een fysische mix van twee of meer stoffen.
Een belangrijk element voor de vorming van metalen is ijzer. Hoewel dit in zuivere vorm een vrijwel onbruikbaar metaal is, worden de eigenschappen veel beter bij toepassing als legering. IJzer is van nature vrij zacht en bros, maar wanneer hier bijv. koolstof aan wordt toegevoegd, ontstaat een sterk materiaal dat beter bekend is als staal.
Technische materialen worden in twee groepen ingedeeld. Ferrometalen (materiaal met als hoofdbestanddeel ijzer) en non-ferrometalen (materiaal met een ander hoofdbestanddeel).
Ferrometalen
Ferrometalen zijn metalen met als hoofdbestandsdeel ijzer (Fe). In deze categorie vallen ijzer, gietijzer en RVS.
Staal is de meest gangbare ferro-metaal. Dit metaal bevat als hoofdbestandsdeel ijzer in combinatie met koolstof. Het koolstof gehalte is vaak niet meer dan 2%. Staal is een kneedproduct dat gevormd kan worden door middel van walsen of smeden. Indien staal wordt uitgevoerd met een koolstofpercentage van 0,2 tot 0,5 is het ook te gieten, dit heet dan gietstaal.
Gietijzer
Gietijzer is een metaal bestaande uit ijzer, koolstof, silicium en andere elementen. Het koolstofpercentage ligt tussen de 2,5% en 4%. Voordeel van dit materiaal is dat het gemakkelijk is te gieten. Producten kunnen dan met behulp van een mal gecreëerd worden.
RVS bestaat uit een combinatie van ijzer, chroom en andere elementen die bestand zijn tegen corrosie. RVS heeft minimaal een chroom gehalte van 10,5%. RVS wordt gebruikt voor constructies die bestand moeten zijn tegen corrosie.
Non-ferrometalen
Non-Ferrometalen zijn metalen waarin geen ijzer aanwezig is, of waarin ijzer niet het hoofdbestandsdeel is. In deze categorie vallen o.a. aluminium en koper, maar ook lood, zink, brons en messing.
Aluminium
Aluminium (Al) wordt zowel in zuivere vorm en als legering toegepast. Aluminium bestaat uit het gelijknamige element en wordt gewonnen uit aluminiumoxide. Aluminium heeft een lage dichtheid en is ideaal voor het realiseren van lichte constructies. Aluminium wordt ook toegepast als legering samen met silicium, kopen en magnesium.
Koper
Koper (Cu) komt veel voor in zuivere vorm. Koper heeft uitstekende geleidingseigenschappen en wordt veel gebruikt voor elektriciteit- en warmtegeleiding. Ook koper wordt in legeringen gebruikt. Een combinatie van koper en tin geeft brons en een combinatie van koper en zink geeft messing.
Heeft u vragen? Neem gerust contact met ons op, wij staan voor u klaar
Productie van metaal
Metalen worden zelden in zuivere vorm gevonden. De meeste metalen worden gedolven uit de natuur, dit wordt ook wel erts genoemd. Ertsen zijn metalen in een verontreinigde toestand, vaak is dit zuurstof. Enkele metalen kunnen in zuivere vorm gevonden worden. Dit zijn bijvoorbeeld: goud, zilver en koper.
Ertsen worden gedolven uit de natuur , vaak in mijnen. Na delving maakt het erts een flotatie- en een pelletiseerproces door. Hierdoor wordt ijzererts omgevormd naar knikkers met een hoog ijzergehalte. De knikkers worden verscheept naar hoogovens. De hoogovens werken bij een temperatuur van 2.000°C. De ijzerhoudende knikkers worden aan de bovenzijde de hoogoven ingevoerd waarna door een chemisch proces gesmolten ijzer ontstaat onderin de hoogoven. Het metaal heeft dan nog geen vorm. Door middel van gieten en walsen wordt het metaal vormgegeven. Het residu wat overblijft wordt slak genoemd en wordt o.a. gebruikt in de wegenbouw.
Structuur van metaal
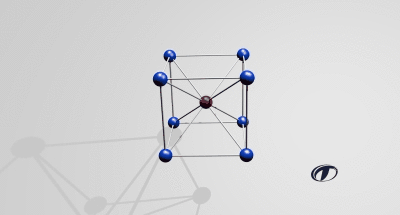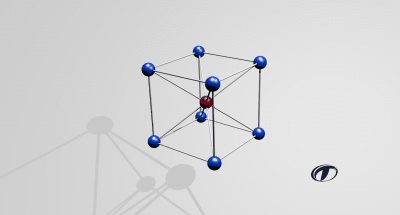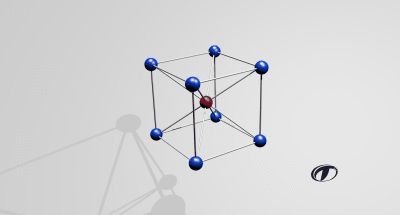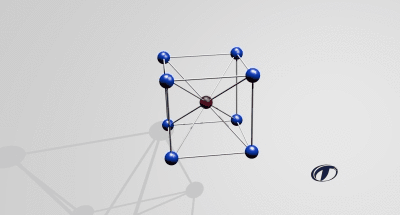
Wanneer een metaal afkoelt vind de overgang van een vloeibare naar vaste fase plaats. Hierbij ontstaat een kristalrooster. Dit kristalrooster komt voor in verschillende structuren; kubisch ruimtelijk gecentreerd (BCC, Body Centered Cubic), kubisch vlakken gecentreerd (FCC, Face Centered Cubic) en hexagonaal dicht gestapeld (HCP, Hexagonal Closest Packed). Het rooster geeft aan hoe de onderlinge kristallen van elkaar zijn gepositioneerd, dit rooster is heel erg klein. Een kristalrooster is nooit volledig zuiver en zal na het stollen altijd fouten bevatten. Men spreekt over: puntfouten, lijnfouten, oppervlaktefouten of volume fouten.
Metaal harden
Deze fouten worden ook wel dislocaties genoemd en hebben sterke invloed op de sterkte van het staal. Veel dislocaties zorgen er namelijk voor dat de kristallen onderling onder spanning komen te staan en niet meer kunnen bewegen. Dislocaties zijn te verwezenlijken door materiaal te rekken (bij het buigen van een paperclip zal het materiaal op de plaats van buiging harder worden, je krijg de paperclip moeilijk tot niet meer exact terug in de oude positie). Daarnaast kan men ook gebruik van andere elementen maken. Door opname van kleine elementen in het kristalrooster tijdens het afkoelen, zal eveneens het rooster onderbreken worden. Dit wordt precipitatieharding genoemd. Als laatste is het ook mogelijk het materiaal af te schrikken (in het Engels: Quenching) om te voorkomen dat de kristallen zich rustig vormen volgens de meest ideale indeling.
Warmtebehandeling van metaal
Door warmtebehandeling zijn de mechanische eigenschappen van metalen te beïnvloeden. Door het metaal te verwarmen kunnen de verschillende stoffen die aanwezig zijn in een legering naar vloeibare toestand gebracht worden. Als het metaal daarna weer afkoelt, is het kristalrooster opnieuw opgebouwd.
De structuur van het materiaal is te beïnvloeden door het reguleren van de afkoelsnelheid. Bij het langzaam afkoelen zijn de verschillende stoffen van de legering goed van elkaar gescheiden. Bij snel afkoelen (schrikken) worden de verschillende stoffen niet goed gescheiden. Daardoor ontstaat een andere structuur.
Tot slot zijn ook de aanwezige stoffen in het metaal te beïnvloeden. Door bijvoorbeeld staal met een maximum percentage koolstof van 2,11% te verwarmen tot boven de 727 °C en vervolgens zeer snel af te schrikken. Het Austeniet krijgt niet de tijd om perliet te vormen en vormt Martensiet, een zeer hard maar bros materiaal. Martensiet is echter zeer bros dus zal voor de bruikbaarheid van het materiaal naderhand nog een extra warmtebehandeling plaats moeten vinden, temperen (Engels: tempered) genoemd, waarbij de hardheid iets afneemt, maar de taaiheid toeneemt.
Voor het afschrikken van metaal kan water of olie gebruikt worden. Water geeft de snelste temperatuurdaling. Gezien deze niet altijd wenselijk is, kan ook olie gebruikt worden.
Bekijk ook
Aluminium
Aluminium is een 65% lichter metaal en goed beschermd tegen corrosie. Het is bijzonder goed recyclebaar en daardoor relatief milieuvriendelijk.
Lees meerDILLIDUR
Dillidur is een slijtvast staal van de producent Dillinger Hütte met waarden die afgegeven worden in hardheid Brinell met waarden tussen 325 en 600.
Lees meerDILLIMAX
DILLIMAX is een hoogsterkte staal van de Duitse staalfabrikant Dillinger Hütte met en vloeigrens tussen 500 en 1.100 MPa.
Lees meer